

 发布时间:2024/1/22
发布时间:2024/1/22  点击次数:
点击次数:
金属腐蚀是指在环境介质的化学作用下,在和物理、机械或生物学因素的共同作用下金属产生的破坏,即金属在它所处环境的作用下所产生破坏。
本期主要介绍金属在不同环境中的腐蚀,包括在大气中、海水中、土壤中、工业环境以及人体环境中的腐蚀情况。
全球范围大气主要成分几乎不变的,其中的水分含量将随地域、季节、时间等条件而变化。参与大气腐蚀过程的是氧和水气,二氧化碳。根据金属表面的潮湿程度的不同,把大气腐蚀分为三类:
1)干大气腐蚀。干大气腐蚀是在金属表面不存在液膜层时的腐蚀。特点是在金属表面形成不可见的保护性氧化膜(1~10nm)和某些金属失泽现象。如铜、银等在被硫化物污染的空气中所形成的一层膜。
2)潮大气腐蚀。潮大气腐蚀是指金属在相对湿度小于100%的大气中,表面存在肉眼看不见的薄的液膜层(10nm~1μm)发生的腐蚀。如铁没受雨淋也会生锈。
3)湿大气腐蚀。湿大气腐蚀指金属在相对湿度大100%,如水分以雨、雾、水等形式直接溅落在金属表面上,表面存在肉眼可见的水膜(1μm ~1mm)发生的腐蚀。
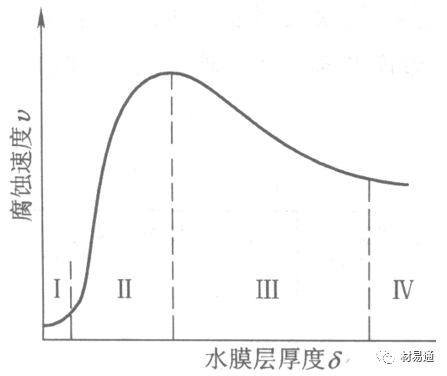
图1大气腐蚀速度与金属表面水膜厚度的关系
根据上图解释腐蚀速度与水膜厚度的规律:
1)区域I 金属表面只有约几个水分子厚(1~10nm)水膜,还没有形成连续的电解质溶液,相当于干的大气腐蚀.腐蚀速度很小。
2)区域II 金属表面水膜厚度约在1μm时,由于形成连续电解液层,腐蚀速度迅速增加,发生潮的大气腐蚀。
3)区域III 水膜厚度增加到1mm时,发生湿的大气腐蚀,氧通过该膜扩散到金属表面显著困难,因此腐蚀速度明显下降。
4)区域IV 金属表面水膜厚度大于1mm,相当于全浸在电解液中的腐蚀,腐蚀速度基本不变。
通常所说的大气腐蚀是指在常温下潮湿空气中的腐蚀。
大气腐蚀机理
大气腐蚀特点是金属表面处于薄层电解液下的腐蚀过程,腐蚀规律符合电化学腐蚀规律。
当金属表面形成连续的电解液薄层时,大气腐蚀的阴极过程主要是氧去极化。
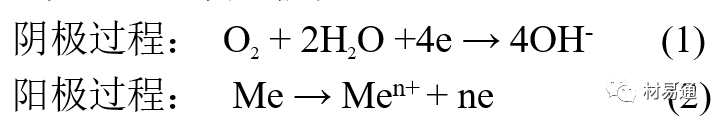
铁、锌等金属全浸在还原性酸溶液中,阴极过程主要是氢去极化,城市污染的大气所形成的酸性水膜下,这些金属的腐蚀主要是氧去极化腐蚀。
在薄液膜下,阳极过程受较大阻滞,氧更易到达金属表面,生成氧化膜或氧的吸附膜,使阳极处于钝态。阳极钝化及金属离子化过程困难造成阳极极化。
当液膜增厚,相当于湿的大气腐蚀时,氧到达金属表面有一个扩散过程,腐蚀过程受氧扩散过程控制。
潮的大气腐蚀主要受阳极过程控制; 湿大气腐蚀主要受阴极过程控制。
大气腐蚀条件不同,锈层成分和结构是很复杂的。Evans认为大气腐蚀的锈层处在潮湿条件下,锈层起强氧化剂作用,在锈层内阳极反应发生在金属/Fe3O4界面上:
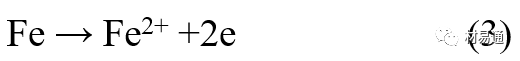
阴极反应发生在Fe3O4/FeOOH界面上:
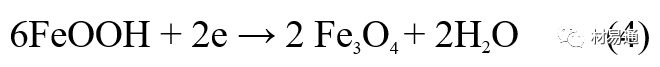
锈层参与了阴极过程,图2为Evans锈层模型图。
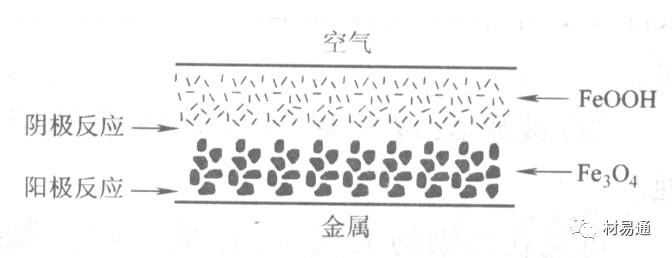
•由图可见,锈层内发生Fe3+→Fe2+的还原反应,锈层参与了阴极过程。
•锈层干燥时,外部气体相对湿度下降时,锈层和底部基体钢在大气中氧的作用下,锈层重新氧化成Fe3+的氧化物,在干湿交替的条件下,锈层加速钢腐蚀过程。•碳钢锈层结构一般分内外两层:
•内层紧靠钢和锈的界面上,附着性好,结构较致密,主要由致密的带少许Fe3O4晶粒和非晶FeOOH构成;
•外层由疏松的结晶α-FeOOH和γ-FeOOH构成。
锈层生成的动力学如图3所示,其曲线遵循幂定律;

P—失重量;K—常数;t—暴露时间;n—常数。
上式也适用于钢的镀锌和镀铝层及W(A1)=55%的Al-Zn镀层的大气试验数。
工业大气中金属腐蚀特点
工业大气中的SO2、NO2、H2S、NH3等都增加大气的腐蚀作用,加快金属的腐蚀速度.
石油、煤等燃科的废气中含SO2最多,在城市和工业区SO2的含量可达0.1~100mg/m3。
常用金属在不同大气环境中的平均腐蚀速度。
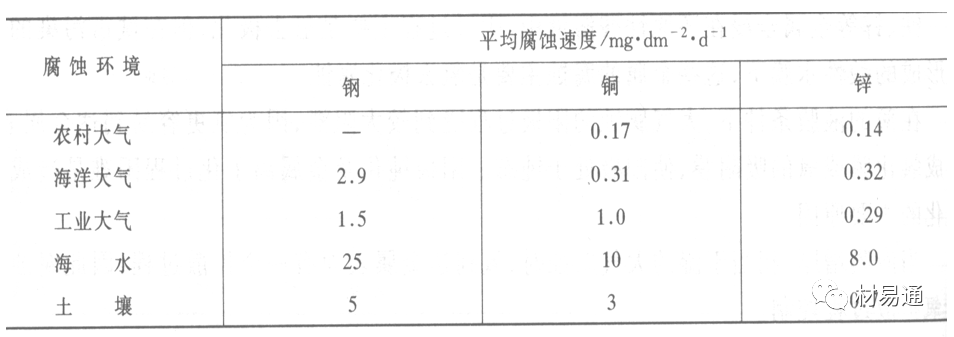
1)Air很纯时,腐蚀速度很小,随湿度增加仅有轻微增加。
2)在污染的空气中,空气相对湿度低于70%时,即便长期暴露,腐蚀速度也是很慢。但SO2有存在的条件下,当相对湿度略高于70%时,腐蚀速度急剧增加。
3)被硫酸铵和煤烟粒子污染的空气加速金属腐蚀。
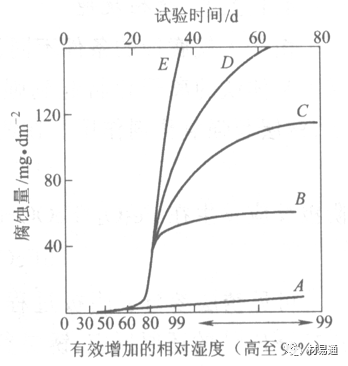
图中A-纯净空气, B-有(NH4)2SO4, C-0.01%SO2, D-(NH4)2SO4+0.01%SO2, E-烟粒+0.01%SO2。
•污染Air,低于临界湿度,金属表面没有水膜,金属受化学作用引起的腐蚀,腐蚀速度很小。高于临界湿度,水膜的形成,电化学腐蚀,腐蚀速度急剧增加。
•大气中SO2对不耐H2SO4腐蚀的金属,如Fe、Zn、Cd、Ni的影响十分明显。呈直线关系上升。
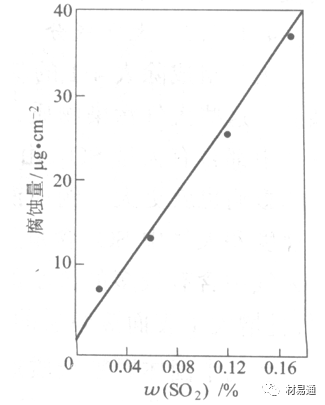
SO2促进金属大气腐蚀的机制
•SO2的腐蚀作用机制是硫酸盐穴自催化过程。
•SO2促进金属大气腐蚀的机制,主要有两种方式:
•一是部分SO2在空气中能直接氧化成SO3,SO3溶于水形成H2SO4;
•二有一部分SO2吸附在金属表面上,与Fe作用生成易溶的硫酸亚铁,FeSO4进一步氧化并由于强烈的水解作用生成了H2SO4,H2SO4再与Fe作用,按这种循环方式加速腐蚀。
•整个过程具有自催化作用,即所谓锈层中硫酸盐穴的作用。
锈层中硫酸盐穴的作用
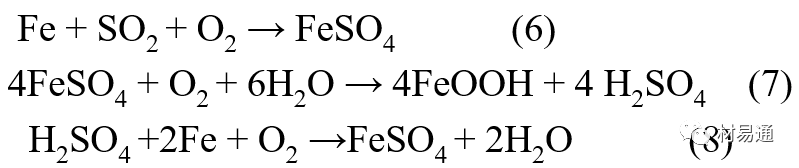
•Schwarz:锈层内FeSO4生成机构如图下所示的模型。锈层的保护能力受其形成时占主导地位的条件影响。如生成的锈层被硫酸盐侵蚀,锈层几乎无保护能力。相反,如最初锈层很少受硫酸盐污染,其保护性较好。
影响大气腐蚀的因素及防蚀方法
•湿度
湿度是决定大气腐蚀类型和速度的一个重要因素。把大气腐蚀速度开始剧增时的大气相对湿度值称为临界湿度。对于铁、钢、铜、锌,临界湿度约在70%~80%之间。由图7可见,湿度小于临界湿度,腐蚀速度很慢,几乎不腐蚀。若把湿度降至临界湿度以下,可防止金属发生大气腐蚀。
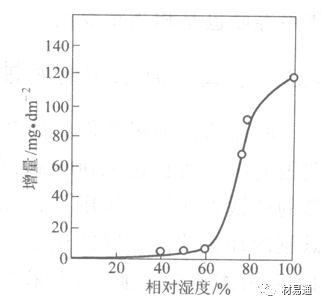
图7 铁在质量分数为0.01%的SO2的空气中经55天后
•大气成分
地理环境不同,有SO2、H2S、NaCl及尘埃等杂质。它们不同程度地加速腐蚀。特别是SO2。煤、石油燃烧的废气中都含有大量SO2, 冬季燃料消耗多,SO2污染更严重,对腐蚀的影响也就更大。
铁、锌等金属在SO2大气中生成易溶的硫酸盐化合物,它们的腐蚀速度和大气中SO2含量呈直线关系上升。
海洋大气中含有较多的微小的NaCl颗粒,它们落在金属的表面上,有吸湿作用,增大了表面液膜层的电导,氯离子本身有很强的侵浊性,因而使腐蚀变得更严重。
大气中固体颗粒称为尘埃。其组成复杂,除海盐粒外,还有碳和碳化物、硅酸盐、氮化物、铵盐等固体颗粒。城市大气中尘埃含量约2mg/m3,工业大气中的尘埃甚至可达1000mg/m3以上。
尘埃对大气的影响有以下几点:
1)尘埃本身具有腐蚀性,如铵盐颗粒能镕入金属表面的水膜,提高电导或酸度促进腐蚀。
2)尘埃本身无腐蚀作用,但能吸附腐蚀物质,如碳粒能吸附SO2和水气生成腐蚀性的酸性溶液。
3)尘埃沉积在金属表面形成缝隙而凝聚水分,形成氧浓差引起缝隙腐蚀。
露置在大气环境中的金属构件和仪器设备应当防尘。
防止大气腐蚀的方法:
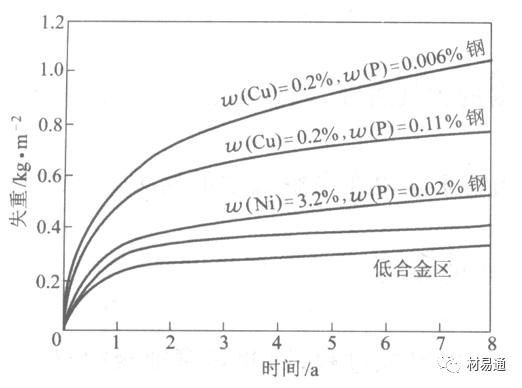
1)提高金属材料的耐蚀性 在碳钢中加入Cu、P、Cr、Ni及稀土元素可提高其耐大气腐蚀性能。例如,美国的Cor-Ten钢(Cu-P-Cr-Ni系低合金钢),其耐大气腐蚀性能为碳钢的4~8倍。
2)采用有机和无机涂层及金属镀层。
3)采用气相缓蚀剂。
4)降低大气湿度, 主要用于仓储金属制品的保护。
•合理设计构件.防止缝隙中存水,去除金属表上的灰尘等都有利于防蚀, 开展环境保护,减少大气污染,不仅有利于人民健康, 而且对延长金属材料在大气中使用寿命也是相当重要的。